Hoe wordt eiwit getest met een stikstof- en aminozuuranalyse?
Bij een meting van het stikstofgehalte op een eiwitshake zijn er 2 methodes die gebruikt kunnen worden; de Kjeldahl en Dumas methode. Bij beiden wordt het stikstof uit de aminozuren vrijgemaakt waaruit men het eiwitgehalte kan berekenen. Ze hebben elk hun voordelen en nadelen bij het meten van whey producten. Bij deze methodes is het nadeel dat afzondelijke aminozuren of stikstofhoudende producten het ewitgehalte hoger kunnen brengen. Dit komt omdat elk aminozuur stikstof bevat dat niet te onderscheiden is op deze manier. Dan is er ook nog de vraag of er op ruw eiwit of droge stof is gemeten en berekend.
Aminozuuranalyse Eiwitshakes
Een geheel andere analyse, een aminozuuranalyse, komt daarom altijd van pas. Dit is de enige manier om kunstmatige toevoeging van stikstofhoudende stoffen zoals losse aminozuren, creatine en collageen uit te sluiten. Elke soort whey eiwit bevat een specifieke verhouding tussen zijn aminozuren. Om deze reden zal een toevoeging van afzonderlijke aminozuren of een uit aminozuur samengesteld product altijd gedetecteerd worden. Ook kunnen we dan zien of er een goedkoper eiwit product toegevoegd is.
Een betere methode voor het onderscheiden van inviduele aminozuren is een meting op niet-gebonden aminozuren. Op deze manier bestaat er geen twijfel of het om een natuurlijke afwijking of toevoeging gaat dmv amino spiking.
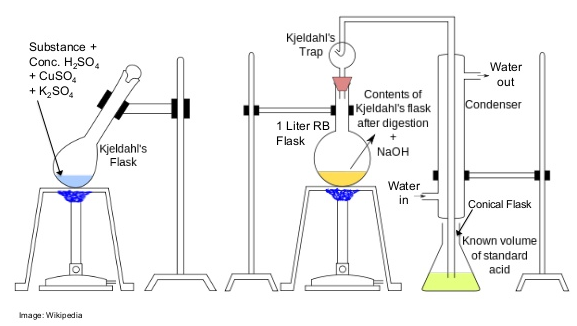
Methode Kjeldahl (stikstofanalyse)
Bij deze methode wordt eerst zwavelzuur toegevoegd om de organische verbindingen (aminozuren) af te breken. Daarna voegt men natriumhydroxide (loog) toe om het stikstof dat vrijkomt om te zetten in ammoniak. Het vrijgekomen ammoniak wordt gemengd met een boorzuur oplossing en hier voegt men dan zoutzuur aan toe. Aan de hand van de metingen tijdens het proces kan het stikstofgehalte berekend worden. Hieruit verder kan het ruw eiwitgehalte voor melkproducten zoals whey berekend worden door met een stikstoffactor van 6,38 te vermenigvuldigen.
Het hele proces duurt een paar uren met een hoop chemisch afval wat niet al te prettig is om mee te werken. Maar het is de goedkoopste en accuraatste manier momenteel. Tegenwoordig zijn er ook Kjeldahl analyse apparaten die vrijwel automatisch werken wat een hoop tijd bespaard en de veiligheid verhoogt.
Automatisch Kjeldahl analyse apparaat

Methode Dumas (stikstofanalyse)
Deze analyse verloopt volautomatisch door middel van een Dumas-analyse apparaat. Het apparaat gebruikt hitte om de stikstofverbindingen te ontleden. Eerst wordt de whey bij 1100ºC verbrand daarna worden de vrijgekomen stikstofverbindingen omgezet naar stikstofoxide (NO2) bij 750ºC. De waterdamp wordt verwijderd en in de laatste fase wordt de NO2 omgezet naar distikstof (N2) bij 600ºC. Nu wordt het gas gefiltert en uiteindelijk gemeten door middel van een gaschromatograaf.
Dit proces duurt ongeveer 4 minuten. Het probleem van deze methode is de prijs van het apparaat en het onderhoud. De kosten komen hierdoor nog een stuk hoger gezien bepaalde onderdelen regelmatig vervangen moeten worden, alsook moet de machine na elke analyse gereinigd worden. Er zou mogelijk ook een grotere kans op afwijkende metingen bestaan. Om deze redenen geniet de Kjeldahl methode voorkeur bij het meten van het eiwitgehaltes in whey producten.

Aminozuuranalyse uitleg
Hiervoor wordt een massaspectrometer gebruikt om elk aminozuur afzonderlijk te 'meten'. Dit wordt gedaan door de gevonden stoffen (aminozuren) te vergelijken met een databank van gekende stoffen. Door middel van chomatografie worden eerst alle stoffen gescheiden tot men alleen het eiwit over heeft. Whey eiwit, zoals elk eiwit, bestaat uit peptides. Dit zijn verschillende aminozuren aan elkaar gelinkt. En elke peptide is dan weer aan elkaar gelinkt om zo een eiwit te vormen.
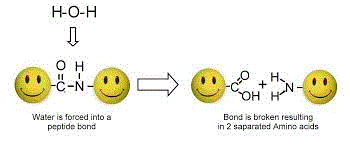
Door middel van hydolysatie worden eerst de peptides van elkaar gescheiden en uiteindelijk de aminozuren door verdere hydrolyse . De massa van elk aminozuur kan worden gedetecteerd door de massaspectrometer en wordt dan vergeleken met de databank. Nadien bepaald men het aantal van elk aminozuur, door dan alle gevonden aminozuren op te tellen kom je het totale eiwitgehalte. Deze methode is natuurlijk het duurste en neemt het meeste tijd in beslag. Maar het is dus de enige manier om 'amino spiking' of toevoeging van andere stikstofhoudende stoffen uit te sluiten.
Op deze manier kunnen ook alle niet-gebonden (vrije) aminozuren gemeten worden om zo amino spiking te detecteren. Hydrolyse komt bij deze meting niet van pas zodat alleen de al mogelijk aanwezige losse aminozuren gemeten worden. Maar toegevoegde creatine of collageen zijn dan niet te onderscheiden van whey eiwit omdat de aminozuren van deze stoffen gebonden zijn.
Massaspectrometer

Voorbeeld analyse
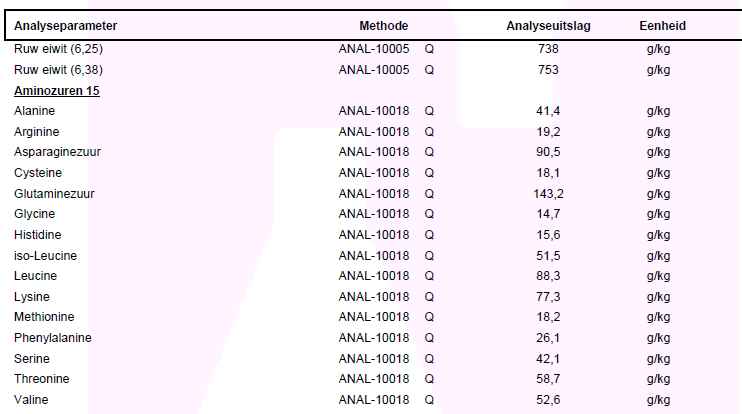
Hieronder een voorbeeld van een Kjeldahl stikstofanalyse en een aminozuuranalyse op 15 aminozuren. Waarom geen 18 kan u hier lezen. De correcte berekening voor de stikstofanalyse van whey is Ruw eiwit (6,38). De waardes zijn in gram per kilogram. Door een komma voor het laatste cijfer te zetten wordt dit het percentage. 75,3% wordt dit dan voor ruw eiwit.
Een afwijking van maximaal 7% (ruw eiwit) ten opzichte van de waarde aangegeven op het label is normaal. Voorbeeld: Als 80% eiwit op het etiket is gedeclareerd -> ((75,3 - 80) / 80) x 100 = -5,9%, dus binnen de toegelaten maximum grens.
Relevante lectuur:
Total Protein Methods and Their Potential Utility

